La revue « Nature » confirme que les vaccins ARNm sont responsables d’anticorps facilitants et augmentent les risques de contamination
La plus grande revue scientifique au monde, NATURE, confirme ce que France-Soir ne cesse de publier, en relayant les scientifiques : les vaccins ARNm sont responsables d’anticorps facilitants et augmentent les risques de contamination peu après la vaccination https://nature.com/articles/s41598-022-19993-w
Source – Article publié le 16 septembre 2022

Le Dr Jean-François Lesgard de Marseille, en parlait depuis 2020, relayé par France Soir :
(Article très technique)
Le phénomène des anticorps facilitants est-il responsable des cas et des décès observés dans les pays à taux de vaccination élevé ?
Publié par France Soir, le 31 mai 2022.
Auteurs : Jean-François Lesgards, docteur en biochimie, et Annelise Bocquet, docteur en biologie santé

ANALYSE — Le système immunitaire a pour objectif principal de protéger l’organisme des agents pathogènes. Quand un micro-organisme ou un élément potentiellement nocif est détecté, le système immunitaire s’active pour l’éliminer. Les cellules et les molécules de l’immunité, dont les anticorps, reconnaissent le pathogène et enclenchent des mécanismes potentiellement dangereux. En effet, le système immunitaire est complexe et son équilibre fragile. Si cet équilibre est perturbé, alors ce système peut se retourner contre l’individu et le détruire à petit feu. De plus, les pathogènes cherchent à le contourner afin de survivre et de se multiplier. Ainsi, des éléments immunitaires « bénéfiques » peuvent devenir des armes contre l’individu et servir les intérêts des micro-organismes. C’est exactement ce qui se passe avec les anticorps… Ils peuvent être impliqués dans des pathologies auto-immunes comme le lupus érythémateux. Ils peuvent également être « détournés » par les pathogènes, notamment les virus, à leur profit. C’est ce que l’on appelle le phénomène « ADE ».
L’ADE (Antibody-Dependent Enhancement) peut être traduit littéralement par « facilitation par les anticorps » en français. Ce phénomène est induit lorsque l’interaction anticorps/antigène faiblit, soit à la suite d’une perte d’affinité et/ou de spécificité des anticorps pour l’antigène, sorte de signature moléculaire des organismes et microorganismes, soit à la suite d’une diminution de leur concentration.
C’est un principe observé dans la réponse immunitaire médiée par certains virus, environ 40, et à la suite de certains vaccins. Plusieurs mécanismes sont possibles et tous ne sont pas encore totalement compris. Mais, globalement, le phénomène d’ADE surgit dans deux grands cas de figure (Wen et al., 2020) :
1. Quand les anticorps promeuvent l’entrée du virus dans des cellules immunitaires comme les monocytes, les macrophages ou les polynucléaires de l’individu contaminé,
2. Quand les mécanismes immunitaires sont paralysés au profit du virus qui a, alors, toute latitude pour se reproduire et se propager dans l’organisme.
Un anticorps est une glycoprotéine constituée d’une partie fixe, appelée Fc, en charge de certaines fonctions biologiques des anticorps et d’une partie variable appelée Fab. Sans trop entrer dans les détails, le Fab contient le paratope qui reconnaît l’antigène par « complémentarité de forme ». Plus cette complémentarité est forte, plus l’anticorps est spécifique de l’antigène. Quant à l’affinité, elle caractérise la force de liaison entre l’anticorps et l’antigène.
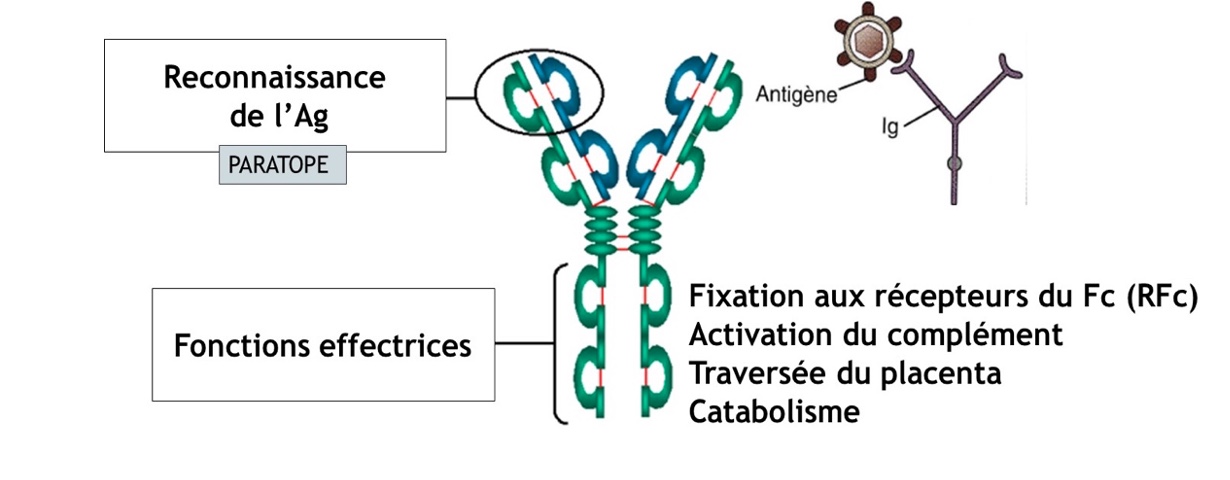
Il est à noter que la partie Fc des anticorps peut également activer le système du complément, notamment le C3 et le C1q (Dustin ML, 2016) (von Kietzell K et al., 2014), deux protéines sériques impliquées dans le phénomène ADE.
Il existe cinq catégories d’anticorps : les IgA (retrouvés dans les muqueuses), les IgM (les premiers anticorps à apparaître en cas d’infection), les IgG (les plus nombreux), les IgE (impliqués dans la réponse immunitaire de type allergique), et les IgD. Dans cet article, pour simplifier, l’attention est portée sur les IgG. Cependant, les IgE peuvent également contribuer à l’ADE (Ricke D.O., 2021), ainsi que les IgM et les IgA (Kulkarni R., 2020).
Deux autres mécanismes interviennent aussi dans la mise en place d’une ADE :
1. Quand l’entrée du virus dans la cellule cible s’effectue par un mécanisme préférentiellement médié par les anticorps, cela bloque la synthèse de médiateurs antiviraux comme le TNFα et l’IFN, ce qui empêche d’alerter le système immunitaire de la présence dudit pathogène et d’enclencher une réponse immunitaire antivirale. En somme, c’est un mécanisme d’échappement immunitaire (Mahalingam and Lidbury, 2002).
2. Quand la liaison de l’antigène viral avec des anticorps induit un changement de conformation de cette molécule. La pénétration du virus dans la cellule cible est alors facilitée si l’antigène ayant subi cette modification est une clé d’entrée cellulaire. Ce mécanisme a été mis en évidence pour le VIH : à la suite de son interaction avec des anticorps monoclonaux en concentration non neutralisante, une des sous-unités du gp120 change de conformation, ce qui permet aux membranes de fusionner. Les anticorps spécifiques anti-gp120 permettent également de réguler l’interaction entre le gp120 et le CCR5, un de ses ligands présent à la surface de cellules immunitaires, ce qui permet au virus d’infecter la cellule. (Guillon et al. 2002) (Wen J et al. 2020).
Normalement, les anticorps opsonisent les pathogènes, c’est-à-dire qu’ils les recouvrent pour les bloquer et permettent ainsi leur élimination par des cellules spécialisées, les phagocytes, que sont les monocytes, les macrophages et les granulocytes (les neutrophiles). Les anticorps, comme les molécules du complément d’ailleurs, sont des opsonines, ce qui signifie « préparer le repas ». De fait, il est possible de comparer la phagocytose à un mécanisme de « digestion » des pathogènes, un mécanisme appelé « microbicidie ».
Pour résumer et schématiser la phagocytose, les opsonines recouvrent les pathogènes, facilitant l’ingestion de l’élément indésirable par le phagocyte qui va le détruire en le « digérant ». Dès la lyse du pathogène terminée, le phagocyte se transforme en CPA (cellule présentatrice d’antigène) via l’apprêtement d’un résidu antigénique issu du pathogène sur le CMHII (Complexe Majeur d’Histocompatibilité), permettant ainsi d’alerter les éléments du système immunitaire adaptatifs, notamment les lymphocytes T helper ou lymphocytes T CD4+. Comme mentionné précédemment, les phagocytes sont, en grande majorité, des monocytes, des macrophages et des granulocytes, des cellules appartenant au système immunitaire inné. La phagocytose est donc un mécanisme pivot entre réponse immunitaire innée et adaptative, un moyen d’enclencher la réponse immunitaire médiée par les lymphocytes.
Pour finir cette petite explication introductive, les phagocytes activés produisent différentes cytokines comme des interleukines (IL-1, IL-6, IL-8, TNF…) et des facteurs de croissance (M-CSF, GM-CSF, G-CSF) qui stimulent la production hématopoïétique des cellules immunitaires myéloïdes (monocytes et granulocytes). Pour information, les cytokines sont responsables de la communication intercellulaire, notamment celles de l’immunité. Elles servent d’alerte pour les effecteurs immunitaires, mais aussi de soutien dans la prolifération, la maturation ou l’activation de ces cellules et dans l’orientation de la réponse immunitaire pour gagner en efficacité face au pathogène. En ce qui concerne l’immunité antivirale, l’interféron représente une famille de cytokines très importante pour diriger la réponse immunitaire envers ces « endoparasites » que sont les virus. (Janis Kuby et al. 7ème édition, Dunod).
Pourquoi faut-il connaître la phagocytose pour comprendre les ADE ?
Pour « manger » puis détruire les pathogènes opsonisés, les phagocytes possèdent des récepteurs à leur surface, leur permettant de reconnaître soit les anticorps via leur partie fixe Fc, soit les complexes C1q/anticorps toujours via le Fc, soit le C3. Ces récepteurs sont :
– les RFcγ (notamment les CD64, CD32 et CD16) pour les IgG (Cloutier M et al. 2020),
– le C1qBP (ou gC1q ou C1qR) et les CR – récepteurs du C1q et du C3 (Anne Nicholson-Weller and Lloyd B Klickstein, 1999) (Webster S.D. et al. 2000).
Pour faire simple, le C1q peut interagir avec la partie constante des anticorps, et médier l’entrée du pathogène dans la cellule cible à l’aide de son récepteur. Il peut aussi activer le système du complément, ce qui aboutit à la formation du C3b qui interagit alors avec son récepteur et induit alors l’entrée du virus dans la cellule présentant des CR à sa surface.
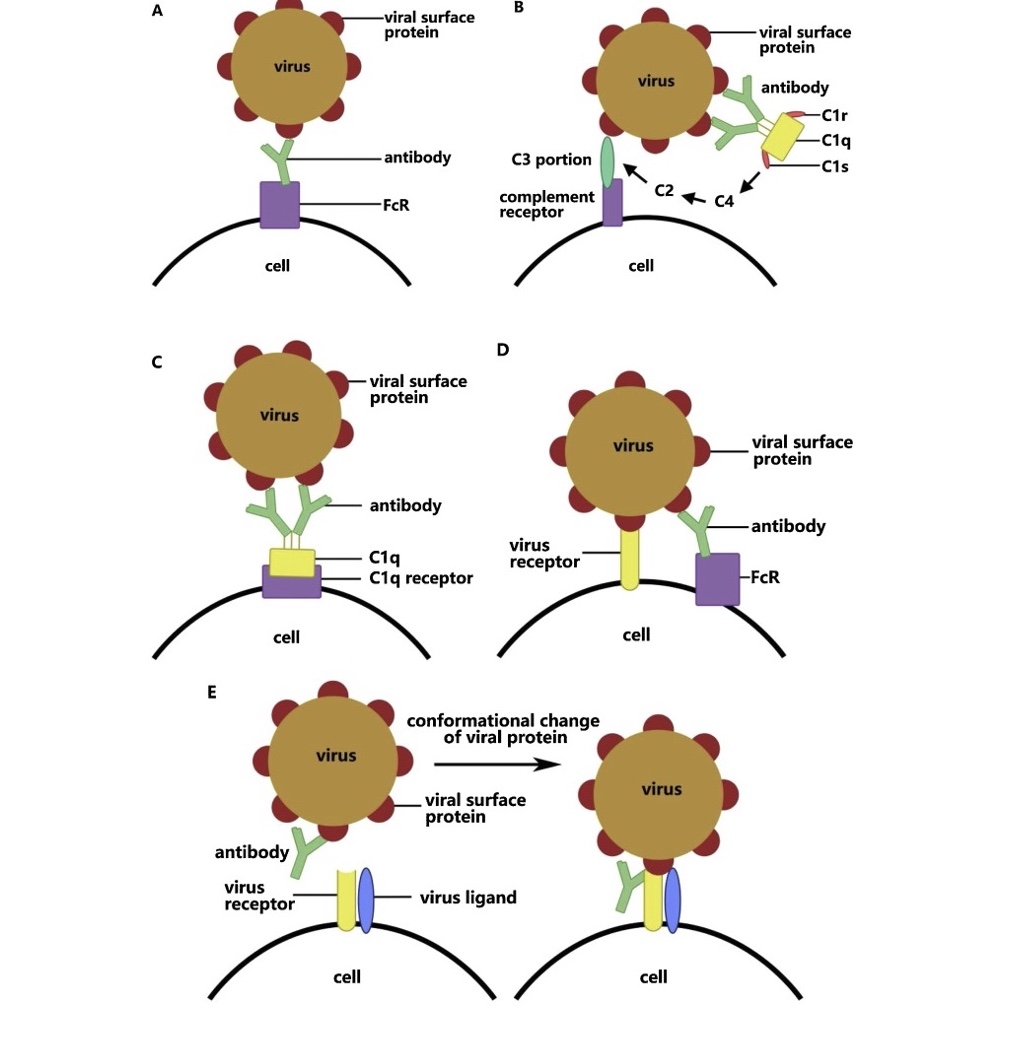
Si l’affinité ou la spécificité des anticorps pour l’antigène diminuent ou que la quantité d’anticorps décroît, les phagocytes internaliseront toujours les éléments pathogènes opsonisés par lesdits anticorps, mais ne les détruiront pas. Les phagocytes véhiculent alors les pathogènes et permettent leur multiplication, ce qui finalement contribue à leur diffusion et non à leur destruction. (Wen et al., 2020).
Ces anticorps peuvent être présents en raison d’une exposition antérieure au virus, d’une exposition à un virus apparenté ou d’une vaccination antérieure contre le virus. Plus en détail, lors de la réinfection, des anticorps en nombre insuffisant ou à la spécificité moindre pour neutraliser le virus se lient néanmoins à sa cible virale. Ces anticorps s’amarrent ensuite au récepteur gamma RFcγII ou CD 32 exprimés sur les cellules immunitaires (globules blancs), facilitant l’entrée virale dans la cellule et augmentant par la suite la charge virale (Wan et. al., 2020). Mieux, dans certains cas – notamment au niveau des poumons, les anticorps non neutralisants peuvent former des complexes immuns avec les antigènes viraux, ce qui induit :
– la sécrétion de cytokines pro-inflammatoires pour recruter des cellules immunitaires susceptibles d’être infectées,
– l’activation du complément et
– le blocage de la sécrétion de médiateurs antiviraux et/ou de l’apoptose cellulaire (Sanchez-Zuno G.A. et al., 2021).
Vous l’aurez compris, l’ADE n’est pas qu’un simple mécanisme facilitant l’entrée du virus dans une cellule immunitaire. Il s’agit d’un ensemble de phénomènes qui permettent à celui-ci d’échapper à la vigilance du système immun, de se multiplier et d’être diffusé dans le corps puisque les cellules immunitaires sont mobiles. Il s’agit d’un véritable « détournement » de cellules immunitaires au profit du virus, ce qui aboutit, en général, à une aggravation de la pathologie.
Historiquement, ce phénomène immunologique a été observé pour la première fois en 1964 (Hawkes et al.,1964). Dans ce travail, Hawkes a décrit une série d’expériences dans lesquelles des cultures de flavivirus (virus transmis par des insectes) ont été incubées avec des sérums de poulets contenant des titres élevés d’anticorps contre ces virus. De façon inattendue, malgré des dilutions de plus en plus élevées de sérums contenant des anticorps, l’infection des cellules cibles du virus a été augmentée. L’absence d’explication est probablement responsable du fait qu’il a été largement ignoré pendant près de 20 ans (Morens et al., 1994).
La production d’anticorps facilitants a été observée dans de nombreuses maladies virales et/ou après vaccination : virus de la dengue (Beltramello et al., 2010), Zika (Bardina et al., 2017) et d’autres flavivirus – virus transmis par des insectes – (Campos et al., 2020), Ebola (Takada et al., 2003), le VIH et des SARS-CoV et MERS-CoV, rougeole, péritonite infectieuse féline, etc. Pour la dengue, les personnes primo-infectées développent une seconde infection plus sévère ayant pour origine l’ADE (Beltramello et al., 2010), ce qui fut également observé chez les personnes précédemment vaccinées contre la maladie (Shukla et al., 2020 ).
Il faut savoir que : « À ce jour, aucune avancée médicale, test immunologique, ou marqueur biologique permet de différencier une infection virale sévère d’une infection virale amplifiée de façon immune, si ce n’est par la mesure des anticorps, des lymphocytes T ou de la réponse intrinsèque de l’hôte (At present, there are no known clinical findings, immunological assays or biomarkers that can differentiate any severe viral infection from immune-enhanced disease, whether by measuring antibodies, T cells or intrinsic host responses.) » (Arvin et al. Nature 2020).
Historique de la recherche sur la vaccination contre les SARS et MERS à partir de protéine N et Spike du virus
Depuis plusieurs décennies, des tentatives de vaccination contre le SARS et le MERS ont été tentées en utilisant essentiellement deux protéines de ces virus : la protéine N (la protéine N est liée à l’ARN du virus qu’elle entoure, nucléocapside hélicoïdale) et la protéine Spike.
Les vaccins à base de protéine N ont très souvent conduit à une aggravation de la maladie avec une inflammation importante et des symptômes respiratoires sévères, voire mortels. Des chercheurs ont montré que l’immunisation vaccinale de souris BALB/c (un modèle animal conventionnel et sensible aux SARS-CoVs) avec la protéine N du SARS-CoV provoque une inflammation pulmonaire grave lors d’un contact ultérieur avec le SARS-CoV, probablement engendrée par un déséquilibre entre activation et suppression des lymphocytes T, ainsi que par la production massive de cytokines pro-inflammatoires (Yasui Fet al., 2010).
Le spécialiste mondial des coronavirus, Ralph S. Baric, ainsi que les auteurs d’une autre étude notent que non seulement la vaccination avec N n’a pas réussi à contrôler la réplication du SARS-CoV dans les poumons, mais qu’elle entraîne une immunopathologie renforcée lors d’une nouvelle infection virale chez les animaux âgés (Deming D et al., 2006). De plus, ils observent que le transfert passif d’anticorps anti-protéine N n’a pas contribué à l’inflammation. Ils ont alors émis l’hypothèse suivante : « en l’absence d’anticorps suffisamment neutralisants, l’activité des lymphocytes T spécifiques à la protéine N du SARS provoque cette réponse inflammatoire dangereuse ». De ce fait, la prudence s’impose en ce qui concerne l’inclusion de la protéine N du SARS-CoV dans toute formulation de vaccin.
Avec le temps, même si des preuves d’amélioration de la maladie semblent s’accumuler avec le vaccin entier inactivé ou le vaccin vectoriel exprimant la protéine N et la protéine S (Lambert PH et al., 2020), les vaccins à base de protéine N restent très risqués (Dolles M et a., 2011). D’ailleurs, d’autres auteurs ont reporté des pneumonies sévères chez des souris vaccinées avec une protéine de nucléocapside après réinfection avec le SARS-CoV1 (Yasui F et al., 2008).
Pour finir, Baric précise dans un autre article : « En outre, la conservation de la protéine N et son implication dans les processus pathologiques évoquent la possibilité d’une immunopathologie dans les populations vaccinées par les souches de coronavirus. La toxicité de la protéine N, et notamment son rôle dans les formes graves et la coagulopathie entraînant la mort, a été clairement établie, y compris dans le SARS-CoV-2 ».
Les vaccins dirigés contre la protéine de pointe (Spike) semblent produire une meilleure immunisation que ceux dirigés contre la protéine N, mais ils peuvent également induire des ADE et aggraver la maladie. En effet, dans une étude, des chercheurs ont constaté que l’ADE associée à l’infection par le SARS-CoV, était principalement médiée par des anticorps anti-Spike (Wang SF et al., 2014). Des sérums prélevés sur des patients infectés par le SARS-CoV affichent une plus grande capacité de neutralisation virale quand ils sont faiblement dilués. En revanche, si les sera sont dilués 1000 à 2000 fois, l’infection par le SARS-CoV est facilitée et provoque des apoptoses cellulaires, c’est-à-dire des lyses cellulaires, plus importantes. Ils concluent ainsi : « les résultats suggèrent que les anticorps dirigés contre les protéines de pointe du SARS-CoV pourraient déclencher des effets ADE. Les données soulèvent de nouvelles questions concernant un vaccin potentiel contre le SARS-CoV, tout en faisant la lumière sur les mécanismes impliqués dans la pathogenèse du SARS. »
Dans un modèle de souris, des expériences de formulation d’un vaccin contre le SARS-CoV-1 ont conduit à une immunopathologie pulmonaire lors d’une infection par le SARS-CoV-1 après les injections (Tseng C-T et al., 2012) (Bolles M et al., 2011). Ces vaccins comprenaient des virus entiers inactivés, des virus inactivés avec adjuvant et un vaccin à protéine de pointe d’ADN recombinant (S) dans une formulation à particules pseudo-virales (VLP). Aussi, des hépatites ont été observées dans le modèle du furet avec le vaccin recombinant Ankara (rMVA) exprimant la protéine Spike du SARS-CoV-1 (Weingartl H et al, 2004). L’ADE a été observée chez les macaques rhésus avec le vaccin anti-SARS-CoV-1 (Wang Q et al., 2016). Enfin, des auteurs ont montré et expliqué que la protéine Spike joue un rôle majeur dans l’ADE du SARS-CoV-1 (Wang S-F et al., 2014) (Karthik K et al., 2020).
Le phénomène d’ADE doit être étudié de façon approfondie pour comprendre les mécanismes conduisant à des formes plus graves de la maladie chez les sujets vaccinés par rapport aux non-vaccinés. En effet, les immunoglobulines G (IgG) préexistants, induits par une vaccination, semblent contribuer à des lésions pulmonaires sévères par les SARS-CoVs comme cela fut observé chez les macaques (Liu et al., 2019).
ADE et vaccination de masse
L’ADE semble se produire plus fréquemment à la suite d’une immunisation vaccinale qu’à la suite d’une infection (Ulrich H et al., 2020) (Lee WS et al., 2020) (Cardozo T et al., 2021). Il est donc essentiel pour les politiques et le public de connaître ce phénomène dans le cadre d’une vaccination à l’échelle mondiale comme celle menée contre le SARS-CoV-2. Certains chercheurs ont essayé d’alerter (qui ? Les autorités ?) sur ce risque majeur comme le professeur Jacques Fantini et directeur de recherche au CNRS Jean-Marc Sabatier (Univ Aix-Marseille) dans l’article du site d’information Info du jour.
Dans le contexte actuel, les campagnes de vaccination consistent à injecter des nanoparticules lipidiques contenant soit l’ARNm (Pfizer et Moderna), soit l’ADN (Janssen et AstraZeneca) de la souche originale du SARS-CoV-2 initial (février 2020) à toute la population. Si les anticorps vaccinaux deviennent inefficaces pour neutraliser le variant Delta ou les autres variants, alors l’infection médiée par ces nouvelles souches virales sera facilitée par les anticorps vaccinaux et les personnes nouvellement infectées peuvent développer une forme plus grave de la maladie.
Les auteurs de cet article ont également publié un travail de modélisation démontrant la diffusion du virus à l’aide d’anticorps dirigés contre la protéine Spike. Ces anticorps « facilitants » ont d’ailleurs plus d’affinités envers la Spike que les anticorps neutralisants en ce qui concerne le variant Delta (contrairement à ce qui est observé avec la souche originale du SARS-CoV-2 de 2020, Wuhan/D614G).
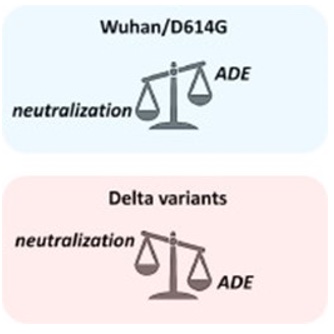

D’où la conclusion des auteurs : « Nous suggérons donc d’évaluer au plus vite, dans les sérums d’individus vaccinés, la balance neutralisation/ADE sur le variant Delta. » (Yahi Net al., 2021).
Cela pourrait expliquer l’inefficacité constatée des vaccins Pfizer et Moderna. En effet, les campagnes vaccinales ont échoué à arrêter les contaminations, et il semble qu’elles ont même entraîné une flambée des cas comme en Israël après la troisième dose généralisée et la quatrième dose en cours. Des phénomènes identiques ont été observés au Royaume-Uni, en Islande, aux États-Unis, etc. Rappelons qu’il n’est pas recommandé, voire dangereux, de vacciner en pleine épidémie.
Par ailleurs, il est essentiel d’étudier les mutations du virus liées à ces phénomènes dans le cadre d’une vaccination aussi généralisée. Une étude d’épidémiologie moléculaire couplée à l’analyse structurale de la protéine Spike indique que l’équilibre entre les anticorps facilitants et neutralisants chez les personnes vaccinées est en faveur de la neutralisation pour la souche Wuhan, les variantes Alpha et Bêta, mais pas pour les Gamma, Delta, Lambda et Mu (Guérin P et al., 2021). Qu’en est-il pour Omicron ? Il semble que l’évolution du SARS-CoV-2 a considérablement affecté la balance ADE/neutralisation qui est aujourd’hui en faveur de l’ADE. Les auteurs insistent à juste titre sur le fait que les futurs vaccins devraient tenir compte de ces données pour concevoir de nouvelles formulations adaptées aux variants du SARS-CoV-2 et dépourvues d’épitopes ADE dans la protéine de pointe (Guérin P et al., 2021) (Zhou Y et al., 2021).
D’autres chercheurs alertent sur le sujet. Dans une correspondance publiée dans Nature Biotechnology, Eroshenko et. al. font un examen des éléments suggérant que l’ADE peut se manifester dans le cadre d’une vaccination employée contre le SARS-CoV-2 (Eroshenko et. al., 2020). Ils rappellent que l’ADE a été observée avec des vaccins contre les coronavirus testés, dans des modèles in vitro et in vivo (Eroshenko et al., 2020). Dans le cas d’un vaccin contre le SARS-CoV-2, les anticorps non neutralisants sont aussi susceptibles de provoquer une forme plus grave de la maladie au lieu de protéger contre le virus, en formant des complexes immuns avec des antigènes viraux pour provoquer une sécrétion excessive de cytokines pro-inflammatoires et, dans le cas extrême, une tempête cytokinique provoquant des lésions tissulaires (Lee et al.,2020). Cela impacte notamment les personnes âgées, les plus susceptibles de développer des formes graves. En effet, Peron et Nakaya fournissent des preuves suggérant que les personnes âgées ayant subi des expositions répétées à des coronavirus peuvent être prédisposées à l’ADE lors d’une contamination au SARS-CoV-2 (Peron JPS and Nakaya H, 2020).
Un article en preprint rapporte que le plasma de 76% des patients rétablis d’un COVID-19 sévère, ajouté à des cultures de virus et de cellules sensibles, augmente l’infectivité par le SARS-CoV-2 des cellules Raji (Wu et al., 2020). Les auteurs notent que les niveaux d’anticorps contre la protéine Spike étaient plus élevés chez les patients âgés de COVID-19, et qu’une réponse des anticorps plus forte était associée à une clairance virale retardée et à une gravité accrue de la maladie chez les patients. Il est donc raisonnable de supposer que les anticorps spécifiques anti-S peuvent contribuer à la gravité de la maladie lors de l’infection par le SARS-CoV-2. (Wu et al., 2020).
Avec les injections « rappel » ou « boosters », il est possible de promouvoir une future infection par le SARS-CoV-2 via un mécanisme « ADE », y compris chez une population plus jeune (Zaman 2021). En outre, il fut constaté que les anticorps monoclonaux humains anti-Spike produisaient des niveaux élevés d’anticorps à réaction croisée contre les protéines humaines endogènes (Vojdani et al., 2021). Il est aussi fort probable que la réplication du virus soit amplifiée, donnant lieu à des effets secondaires. D’excellentes revues ont montré la possibilité d’ADE dans le SARS-CoV-2 notamment à la suite de la vaccination dirigée contre la protéine Spike (Arvin et al. 2020) (Lee WS et al., 2020) (Bournazos S, et al., 2020). Étant donné que les macrophages/monocytes expriment les RFcγ à leurs surfaces (Bournazos S, et al., 2020) (Bruhns P, 2012) (Klaassen RJ et al., 1990), les macrophages sont considérés comme les principaux inducteurs d’ADE. De plus, l’hyper-inflammation est souvent causée lors d’ADE par les cellules immunitaires, y compris les macrophages, dans diverses infections virales (Maemura T et al., 2021) (Cloutier M et al., 2020).
Le phénomène d’ADE peut être plus ou moins conséquent. Des auteurs stipulent, dans une de leurs études, avoir observé l’ADE en utilisant du plasma de sujets atteints de COVID-19 en phase de convalescence et des cellules BHK exprimant les récepteurs RFcγ humains. Ils ont constaté que certains récepteurs médiaient une ADE modeste au niveau de l’infection contre le SARS-CoV-2 (Maemura T et a., 2021). Une augmentation faible de l’infection a été observée dans les macrophages infectés par le SARS-CoV-2 associé à peu d’inflammation et d’expression de cytokines/chimiokines pro-inflammatoires. L’infection par le SARS-CoV-2 produit ainsi des anticorps qui déclenchent l’ADE, mais ces anticorps ne contribuent pas à la production excessive de cytokines par les macrophages dans ce cas.
[…]
Conclusion
Avec de multiples boosters, le rapport bénéfice/risque peut devenir défavorable pour les vaccins en induisant notamment des processus ADE, surtout si les variants s’éloignent de la souche virale originale du SARS-CoV-2 servant à formuler les vaccins.
En cherchant à produire des anticorps neutralisants en abondance, on risque la production d’anticorps facilitants menant au déclenchement d’ADE. Plutôt qu’une protection vaccinale, on se retrouve avec une infection cellulaire facilitée. Les personnes infectées par les nouveaux variants peuvent par conséquent développer une maladie plus grave que les personnes non vaccinées. Heureusement, le variant « Omicron », hautement contagieux, est majoritaire dans le monde entier. Il présente une létalité 7 fois moindre que le variant Delta qui est lui-même 4 fois moins létal que la souche originale de Wuhan. L’émergence de variants du SARS-CoV-2 toujours moins létaux, bien que plus contagieux, rend le phénomène ADE moins problématique.
Mais, en tenant compte de tous les éléments précités, il y a des raisons suffisantes de soupçonner que les anticorps dirigés contre la protéine Spike contribuent et contribueront aux phénomènes d’ADE provoqués par une infection faisant suite à une vaccination. Cela peut se manifester par des affections auto-immunes et inflammatoires aiguës ou chroniques aggravant la sévérité de la maladie et la situation pandémique globale.
Une chose est sûre, le gouvernement et le Haut Conseil de la santé publique (HCSP) n’ont nullement intérêt à ce que l’effet ADE des anticorps facilitants puisse être mis en évidence dans les pays ayant pratiqué la vaccination à outrance comme la France. Les experts du HCSP ne peuvent nier être informés des tentatives « vaccinales » après la pandémie de SARS-CoV de 2003, ce qui a mis en évidence le risque d’ADE, en particulier chez les sujets âgés. Cela a pu motiver, entre autres, l’extrême opacité des chiffres concernant le statut vaccinal et le type de variant caractérisant les personnes admises en réanimation ou en soins critiques.
Références :
Arvin AM, Fink K, Schmid MA, Cathcart A, Spreafico R, Havenar-Daughton C and Virgin HW. (2020). A Perspective on Potential Antibody-Dependent Enhancement of SARS-CoV-2. Nature 584(7821): 353-363.
Bardina SV, Bunduc P, Tripathi S, Duehr J, Frere JJ, Brown JA and Lim JK (2017). Enhancement of Zika Virus Pathogenesis by Preexisting Antiflavivirus Immunity. Science 356(6334): 175-180.
Beltramello M, Williams KL, Simmons CP, Macagno A, Simonelli L, Ha Quyen, NT and Sallusto F (2010). The Human Immune Response to Dengue Virus is Dominated by Highly Cross-Reactive Antibodies Endowed with Neutralizing and Enhancing Activity. Cell Host Microbe 8(3): 271-83.
Bolles M, Deming D, Long K, Agnihothram S, Whitmore A, Ferris M, et al. A double-inactivated severe acute respiratory syndrome coronavirus vaccine
provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge. J Virology. (2011)
85:12201–15. doi: 10.1128/JVI.06048-11
Bournazos S, Gupta A, Ravetch JV. 2020. The role of IgG Fc receptors in antibody- dependent enhancement. Nat Rev Immunol 20:633–643.
Campos J, Slon L, Mongkolsapaya J, & Screaton GR (2018). The Immune Response Against Flaviviruses. Nature immunology 19(11): 1189-1198.
Bruhns P. 2012. Properties of mouse and human IgG receptors and their contribution to disease models. Blood 119:5640–5649.
Cardozo T, Veazey R. Informed consent disclosure to vaccine trial subjects of risk of COVID-19 vaccines worsening clinical disease. Int J Clin Pract. 2021 Mar;75(3):e13795.
Cloutier M, Nandi M, Ihsan AU, Chamard HA, Ilangumaran S, Ramanathan S. 2020. ADE and hyperinflammation in SARS-CoV2 infection—comparison
with dengue hemorrhagic fever and feline infectious peritonitis. Cytokine 136:155256.
Deming D, Sheahan T, Heise M, Yount B, Davis N, Sims A, Suthar M, Harkema J, Whitmore A, Pickles R, West A, Donaldson E, Curtis K, Johnston R, Baric R. Vaccine efficacy in senescent mice challenged with recombinant SARS-CoV bearing epidemic and zoonotic spike variants. PLoS Med. 2006 Dec;3(12):e525. doi: 10.1371/journal.pmed.0030525
Dolles M, Deming D, Long K, Agnihothram S, Whitmore A, Ferris M, Funkhouser W, Gralinski L, Totura A, Heise M, Baric RS. A double-inactivated severe acute respiratory syndrome coronavirus vaccine provides incomplete protection in mice and induces increased eosinophilic proinflammatory pulmonary response upon challenge. J Virol. 2011 Dec;85(23):12201-15.
Dustin ML, Complement receptors in myeloid cell adhesion and phagocytosis, Microbiol Spectr. 2017 doi: 10.1128/microbiolspec.MCHD-0034-2016
EPV-CoV19 EpiVax’s T Cell Epitope-Driven vaccine for COVID-19 (2020).Available online at: https://epivax.com/pipeline/epv-cov19 (accessed January
28, 2021).
Eroshenko N, Gill T, Keaveney MK, Church GM, Trevejo JM. & Rajaniemi H (2020). Implications of Antibody-dependent Enhancement of Infection for SARS-CoV-2 Countermeasures. Nature Biotechnology 38(7): 789-791.
Guérin P, Yahi N, Azzaz F, Chahinian, Sabatier JM, Fantini J. Distinct evolution of infection-enhancing and neutralizing epitopes in the spike protein of SARS-CoV-2 variants (alpha, beta, gamma, delta, lambda and µ): a structural and molecular epidemiology study. Preprint. Doi: 10.22541/au.163638609.95446888/v1
Hawkes RA (1964). Enhancement of the Infectivity of Arboviruses by Specific Antisera Produced in Domestic Fowls. Australian Journal of Experimental Biology and Medical Science 42(4): 465-482.
Karthik K, Senthilkumar TMA, Udhayavel S, Raj GD. Role of antibody-dependent enhancement (ADE) in the virulence of SARS-CoV-2 and its mitigation strategies for the development of vaccines and immunotherapies to counter COVID-19. Hum Vaccin Immunother. 2020 Dec 1;16(12):3055-3060. doi: 10.1080/21645515.2020.1796425
Klaassen RJ, Ouwehand WH, Huizinga TW, Engelfriet CP, von Dem Borne AE. 1990. The Fc-receptor III of cultured human monocytes. Structural
similarity with FcRIII of natural killer cells and role in the extracellular lysis of sensitized erythrocytes. J Immunol 144:599–606.
Kuby J., Owen J.A., Punt J., Stranfort S.A., “Immunologie” – 7ème édition Dunod, ISBN-10 2100705431 ISBN-13 978-2100705436
Kulkarni R. 2020. Antibody-dependant enhancement of viral infections. Dynamics of Immune Activation in Viral Diseases. Springer Singapore (99-41) ISBN 9789811510441
Lambert PH, Ambrosino DM, Andersen SR, Baric RS, Black SB, Chen RT, Dekker CL, Didierlaurent AM, Graham BS, Martin SD, Molrine DC, Perlman S, Picard-Fraser PA, Pollard AJ, Qin C, Subbarao K, Cramer JP. Consensus summary report for CEPI/BC March 12-13, 2020 meeting: Assessment of risk of disease enhancement with COVID-19 vaccines. Vaccine. 2020 Jun 26;38(31):4783-4791. doi : 10.1016/j.vaccine.2020.05.064
Lee WS, Wheatley AK, Kent SJ, DeKosky BJ. Antibody-dependent enhancement and SARS-CoV-2 vaccines and therapies. Nat Microbiol. 2020 Oct;5(10):1185-1191.
Lisziewicz J, Lori F. Precision COVID-19 vaccine with companion diagnostics. Prec Nanomed. (2020) 3:487–94. doi: 10.33218/001c.12561
Liu L, Wei Q, Lin Q, Fang J, Wang H, Kwok H and Chen Z (2019). Anti — spike IgG Causes Severe Acute Lung Injury by Skewing Macrophage Responses During Acute SARS-CoV Infection. JCI Insight 4(4): e123158.
Lu LL, Suscovich TJ, Fortune SM & Alter G (2018). Beyond Binding: Antibody Effector Functions in Infectious Diseases. Nature Reviews Immunology18(1): 46-61.
Maemura T, Kuroda M, Armbrust T, Yamayoshi S, Halfmann PJ, Kawaoka Y. Antibody-Dependent Enhancement of SARS-CoV-2 Infection Is Mediated by the IgG Receptors FcγRIIA and FcγRIIIA but Does Not Contribute to Aberrant Cytokine Production by Macrophages. mBio. 2021 Oct 26;12(5):e0198721. doi: 10.1128/mBio.01987-21
Mahalingam S. et al. 2002. The viral manipulation of the host cellular and immune environments to enhance propagation and survival : a focus on RNA viruses. Journal of Leukocyte Biology (Vol. 72 429-439)
Morens DM (1994). Antibody-Dependent Enhancement of Infection and the Pathogenesis of Viral Disease. Clinical Infectious Diseases 19(3): 500-512.
Nicholson-Weller A. and Klickstein L.B. 1999. C1q-binding proteins and C1q receptors. Current Opinion in Immunology, 11:42-46. Elsevier Science Ltd ISSN 0952-7915
Peron JPS and Nakaya, H (2020). Susceptibility of the Elderly to SARS-CoV-2 Infection: ACE-2 Overexpression, Shedding, and Antibody-dependent Enhancement (ADE). Clinics (Sao Paulo) 75: e1912.
Ricke DO. Two Different Antibody-Dependent Enhancement (ADE) Risks for SARS-CoV-2 Antibodies. Front Immunol. 2021 Feb 24;12:640093. doi: 10.3389/fimmu.2021.640093
Sanchez-Zuno G.A. et al. 2021. A review : Antibody-dependent enhancement in COVID-19 : The not so friendly side of antibodies. International Journal of Immunopathology & Pharmacology. (Vol. 35 : 1 – 15) doi: 10.1177/20587384211050199
Shukla R, Ramasamy V, Shanmugam RK, Ahuja R & Khanna N (2020). Antibody-Dependent Enhancement: A Challenge for Developing a Safe Dengue Vaccine. Frontiers in Cellular and Infection Microbiology 10: 572681.
Takada A, Feldmann H, Ksiazek TG & Kawaoka Y (2003). Antibody-Dependent Enhancement of Ebola Virus Infection. Virology 77(13): 7539-7544.
Tseng C-T, Sbrana E, Iwata-Yoshikawa N, Newman PC, Garron T, Atmar RL, et al. Immunization with SARS coronavirus vaccines leads to pulmonary
immunopathology on challenge with the SARS virus. PLoS ONE. (2012) 7:e35421. doi: 10.1371/journal.pone.0035421
Ulrich H, Pillat MM, Tárnok A. Dengue Fever, COVID-19 (SARS-CoV-2), and Antibody-Dependent Enhancement (ADE): A Perspective. Cytometry A. 2020 Jul;97(7):662-667.
Vojdani A, Vojdani E & Kharrazian D. (2021). Reaction of Human Monoclonal Antibodies to SARS-CoV-2 Proteins with Tissue Antigens: Implications for Autoimmune Diseases. Frontiers in Immunology 11: 3679.
von Kietzell K, Pozzuto T, Heilbronn R et al. Antibody-mediated enhancement of parvovirus B19 uptake into endothelial cells mediated by a receptor for complement factor C1q. J. Virol. 2014 doi : 10.1128/JVI.00649-14
Wan Y, Shang J, Sun S, Tai W., Chen J, Geng, Q & Li F. (2020). Molecular Mechanism for Antibody- Dependent Enhancement of Coronavirus Entry. Journal of virology, 94(5).
Wang SF, Tseng SP, Yen CH, Yang JY, Tsao CH, Shen CW, Chen KH, Liu FT, Liu WT, Chen YM, Huang JC. Antibody-dependent SARS coronavirus infection is mediated by antibodies against spike proteins. Biochem Biophys Res Commun. 2014 Aug 22;451(2) :208-14. doi: 10.1016/j.bbrc.2014.07.090
Wang Q, Zhang L, Kuwahara K, Li L, Liu Z, Li T, et al. Immunodominant SARS coronavirus epitopes in humans elicited both enhancing and neutralizing effects on infection in non-human primates. ACS Infect Dis. (2016) 2:361–76. doi: 10.1021/acsinfecdis.6b00006
Webster S.D. et al. 2000. Structural and functional evidence for microglial expression of C1qRp, the C1q receptor that enhances phagocytosis. Journal of Leukocyte Biology (Vol. 67, 109-115)
Weingartl H, Czub M, Czub S, Neufeld J, Marszal P, Gren J, et al. Immunization with modified vaccinia virus ankara-based recombinant vaccine against severe acute respiratory syndrome is associated with enhanced hepatitis in ferrets. J Virol. (2004) 78:12672. doi: 10.1128/JVI.78.22.12672-12676.2004
Wen J, Cheng Y, Ling R, Dai Y, Huang B, Huang W, Zhang S, Jiang Y Antibody-dependant enhancement of coronavirus (2020) International Journal of Infectious Diseases 483-489. doi : 10.1016/j.ijid.2020.09.015
Wu F, Yan R, Liu M, Liu Z, Wang Y, Luan D and Huang, J. (2020). Antibody-Dependent Enhancement (ADE) of SARS-CoV-2 Infection in Recovered COVID-19 Patients: Studies Based on Cellular and Structural Biology Analysis. medRxiv preprint.
Yahi N, Chahinian H, Fantini J. Infection-enhancing anti-SARS-CoV-2 antibodies recognize both the original Wuhan/D614G strain and Delta variants. A potential risk for mass vaccination? J Infect. 2021 Nov;83(5):607-635. doi: 10.1016/j.jinf.2021.08.010
Yasui F, Kai C, Kitabatake M, Inoue S, Yoneda M, Yokochi S, et al. Prior immunization with severe acute respiratory syndrome (SARS)-associated coronavirus (SARS-CoV) nucleocapsid protein causes severe pneumonia in mice infected with SARS-CoV. J Immunol. (2008) 181:6337. doi: 10.4049/jimmunol.181.9.6337
Yasui F, Kai C, Saito K, Inoue S, Yoneda M, Morita K, Mizuno K, Kohara M. Analysis of the mechanism by which BALB/c mice having prior immunization with nucleocapsid protein of SARS-CoV develop severe pneumonia after SARS-CoV infection. Procedia Vaccinol. 2010;2(1):44-50. doi: 10.1016/j.provac.2010.03.009.
Zaman M (2021). COVID Vaccine Booster Shots Are Coming — Here’s What to Know. https://www.msn.com/enus/health/medical/covid-vaccine-booster-shots-are-coming-here-s-what-to-know/ar-BB1foY4s. Accessed 5/1/2021.
Zhou Y, Liu Z, Li S, Xu W, Zhang Q, Silva IT, Li C, Wu Y, Jiang Q, Liu Z, Wang Q, Guo Y, Wu J, Gu C, Cai X, Qu D, Mayer CT, Wang X, Jiang S, Ying T, Yuan Z, Xie Y, Wen Y, Lu L, Wang Q. Enhancement versus neutralization by SARS-CoV-2 antibodies from a convalescent donor associates with distinct epitopes on the RBD. Cell Rep. 2021 Feb 2;34(5):108699. doi: 10.1016/j.celrep.2021.108699




