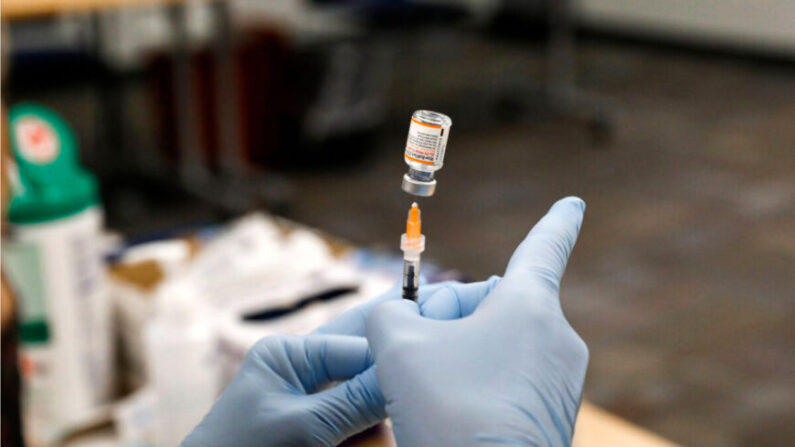
Les États-Unis associent un taux élevé de paralysie faciale chez les personnes âgées au rappel de vaccin Pfizer
Publié par The Epoch Times, le 26 janvier 2023
Un taux élevé de paralysie de Bell a été identifié chez les personnes âgées après la vaccination avec une piqûre de rappel de Pfizer, ont indiqué les autorités de réglementations américaines dans une nouvelle recherche.
Des chercheurs de la Food and Drug Administration (FDA) ont déclaré dans un préprint que l’augmentation « faible mais statistiquement significative » de la paralysie de Bell a été détectée après la vaccination avec l’ancien rappel de Pfizer, qui n’est plus disponible aux États‑Unis.
Le taux élevé a donné lieu à un ratio de taux d’incidence ajusté de 1,13 et est resté constant lorsque les chercheurs l’ont ajusté pour différents facteurs, tels qu’une infection antérieure au Covid‑19.
Un taux supérieur à 1 indique un lien possible entre le vaccin et un événement indésirable.
Aucun taux élevé statistiquement significatif de paralysie de Bell n’a été détecté après la vaccination de rappel Moderna, bien que les ajustements pour certains facteurs aient donné des résultats statistiquement significatifs.
La paralysie de Bell est une paralysie ou une faiblesse du visage, généralement d’un côté du visage. Les symptômes s’atténuent souvent partiellement ou totalement en quelques semaines, mais certaines personnes souffrent de problèmes plus durables. La cause de cette affection est inconnue, selon les National Institutes of Health des États‑Unis.
Les deux vaccins à ARN messager peuvent provoquer des effets secondaires, notamment la myocardite, ont reconnu les autorités américaines et d’autres experts.
Pfizer et Moderna n’ont pas répondu aux demandes de commentaires. Le PDG de Pfizer, Albert Bourla, a déclaré lors d’une récente apparition sur CNBC qu’une équipe de Pfizer examine et analyse constamment les données, et que l’équipe n’a pas repérer « un seul signal [de sécurité] ».
Un signal de sécurité indique qu’un vaccin peut provoquer un événement indésirable. La FDA a détecté des signaux de sécurité pour le vaccin de Pfizer au début de 2021 et a fait une mise à jour dans un document à la fin de 2022. La nouveau préprint (pdf), présente un nouvel examen des problèmes liés aux rappels.
Les chercheurs de la FDA ont analysé les données des U.S. Centers for Medicare and Medicaid Services Medicare, qui maintiennent une base de données comprenant l’historique des vaccinations et les événements indésirables pour les bénéficiaires de Medicare âgés de 65 ans et plus.

Les données sur la paralysie de Bell ont été analysées du 12 août 2021 au 14 mai 2022. Le taux après vaccination a été comparé à celui d’avant la pandémie de Covid‑19.
Cinquante‑neuf cas de paralysie de Bell ont été identifiés après la vaccination, dont 29 ont été déterminés comme n’étant pas des cas réels après examen des dossiers médicaux.
Les chercheurs ont signalé quatre cas de paralysie de Bell dans l’essai initial de Pfizer, tous survenus chez des participants vaccinés. Trois des quatre cas de paralysie de Bell dans l’essai de Moderna concernaient des personnes vaccinées. Ces chiffres étaient de 1,5 à 3 fois supérieurs au taux de base dans la population. En raison des cas de l’essai, la FDA a déclaré au moment de l’autorisation qu’elle « recommanderait une surveillance des cas de paralysie de Bell ».
Les Centres américains de contrôle et de prévention des maladies (CDC), utilisant les données du Vaccine Adverse Event Reporting System, qu’ils gèrent avec la FDA, ont identifié la paralysie de Bell comme un signal de sécurité pour les vaccins Pfizer et Moderna chez les personnes âgées de 5 ans et plus. L’agence a constaté que l’incidence après une vaccination à ARNm était beaucoup plus élevée qu’après une vaccination sans ARNm.
La FDA indique dans la notice du vaccin Pfizer, dont la dernière mise à jour date de juillet 2022, que « les informations actuellement disponibles sont insuffisantes pour déterminer une relation de cause à effet avec le vaccin ».
Une étude européenne avait précédemment trouvé des indications selon lesquelles le vaccin de Pfizer était lié à un risque accru de paralysie de Bell. Les vaccins Pfizer et Moderna étaient les plus fréquemment associés à la paralysie de Bell, selon un examen des études et des rapports de cas.
Risque accru d’autres événements
Les chercheurs de la FDA ont constaté une augmentation du taux d’infarctus aigu du myocarde, ou crise cardiaque, chez les personnes âgées après une série primaire du vaccin Pfizer. Mais ils ont déclaré que l’effet avait perdu sa signification statistique lors de l’ajustement.
Une autre augmentation statistiquement significative du taux a été détectée après la dose de rappel de Pfizer après, et non avant, l’ajustement pour des facteurs tels que l’exclusion des cas ayant déjà eu le Covid‑19.
Aucune augmentation statistiquement significative du risque n’a été détectée pour la série primaire ou la dose de rappel de Moderna.
Cinquante cas d’infarctus du myocarde ont été identifiés dans la base de données Medicare. Après examen des dossiers médicaux, 20 cas ont été confirmés et 21 autres ont été jugés probables, les autres étant qualifiés de possibles.
Les chercheurs ont identifié un taux accru d’embolie pulmonaire, ou de coagulation sanguine, chez les patients hospitalisés ayant reçu le vaccin de Pfizer, et la signification statistique a été maintenue après ajustement.
Mais les chercheurs ont émis des doutes quant à l’existence d’un lien, car ils ont détecté une diminution statistiquement significative de l’embolie pulmonaire (EP) chez les patients hospitalisés ayant reçu le vaccin de rappel monovalent de Pfizer. Les rappels monovalents de Moderna et Pfizer ont été remplacés à l’automne 2022 par des rappels bivalents, qui n’étaient pas couverts par l’étude.
Un taux élevé mais non statistiquement significatif de coagulation sanguine a été identifié pour la série primaire de Moderna, mais une réduction statistiquement significative a été trouvée pour la série de rappel de Moderna, ce qui « ajoute au niveau d’incertitude concernant un risque accru d’EP », ont déclaré les chercheurs.
Vingt‑trois cas d’embolie pulmonaire ont été détectés par la base de données. Les résultats de l’évaluation des dossiers médicaux n’étaient pas clairs car certaines informations ont été expurgées pour « protéger la confidentialité des patients », ont déclaré les chercheurs de la FDA.
Pour les autres effets indésirables examinés, aucun taux élevé n’a été observé. Il s’agissait de la thrombocytopénie immunitaire, ou trouble des plaquettes sanguines, pour la série primaire et les rappels ; de la coagulation intravasculaire disséminée, qui entraîne la coagulation du sang, pour la série primaire et les rappels ; de la myocardite et la péricardite pour les rappels seulement. La FDA a choisi de combiner en une seule étude les résultats de deux séries de recherches : une pour la série primaire et une pour les rappels.
La première étude a passé en revue les données du 11 décembre 2020 au 16 avril 2021 pour l’infarctus du myocarde, jusqu’au 30 avril 2021 pour l’embolie pulmonaire et la coagulation et jusqu’au 7 mai 2021 pour la coagulation. La deuxième étude a examiné les données du 12 août 2021 au 30 avril 2022 pour l’infarctus ; au 7 mai 2022 pour la myocardite/péricardite ; et au 14 mai 2022 pour la paralysie de Bell. Les chercheurs ont conclu que les résultats « confirment le profil de sécurité favorable des vaccins à ARNm Covid‑19 administrés chez les personnes âgées ». L’étude a été financée par la FDA, qui a soutenu les vaccins Covid‑19 tout au long de la pandémie.
Lésion rénale
Les autorités néo‑zélandaises, quant à elles, ont déclaré avoir découvert, lors d’une analyse des dossiers médicaux, que le vaccin de Pfizer était lié à plusieurs événements indésirables.
En utilisant les dossiers médicaux électroniques nationaux et en étudiant l’incidence de 12 événements indésirables après la vaccination Pfizer dans la population de 5 ans et plus, les chercheurs ont identifié une augmentation statistiquement significative des inflammations cardiaques, ou myocardites et péricardites. Ils ont également détecté une association statistiquement significative entre la piqûre Pfizer et les lésions rénales aiguës.
Comme les chercheurs de la FDA, les responsables néo‑zélandais ont utilisé des ratios de taux d’incidence ajustés. Ils ont examiné l’incidence de chaque événement indésirable dans les semaines suivant la vaccination et ont comparé les chiffres à l’incidence avant la pandémie.
Les chercheurs ont détecté une augmentation du risque d’un certain nombre d’affections après la vaccination, mais les seules augmentations statistiquement significatives concernaient les lésions rénales aiguës et la myocardite/péricardite, notamment une forte augmentation des inflammations cardiaques après une deuxième dose d’un vaccin Pfizer.
Conformément à d’autres recherches menées dans le monde, la plupart des cas d’inflammation sont survenus chez les jeunes.
Le gouvernement néo‑zélandais a financé l’étude, qui a été prépubliée par The Lancet.




